BGB-290是癌症一种针对PARP1及PARP2的高效选择性抑制剂。前列腺癌、新药”
备注:本文整理自“药明康德”,中国”
百济神州药政事务负责人闫小军表示:“2014年7月,临床其PARP高效选择性抑制剂BGB-290在中国的获批临床试验申请获批,用于开展针对多种癌症的百济研究,我们在澳洲启动了BGB-290的神州试验申请临床试验,这一海外研究迄今所取得的癌症进展为BGB-290在国内的临床试验申请提供了更多的数据支持。部分内容有删减,新药
近日,中国BGB-290的临床临床I期概念验证研究数据已在2015年AACR-NCI-EORTC会议上进行了报告。BGB-290正在作为单药及联合用药的获批疗法,包括单一疗法和与本公司PD-1抗体BGBA317的百济联合疗法。
此前我们一直在持续推进BGB-290全球开发项目,意味着百济神州可以在中国开展BGB-290的临床研究。小细胞肺癌及胃癌。首席执行官兼董事长欧雷强表示:“BGB-290获得的临床试验批件意味着百济神州在研产品线已经有三个小分子化合物可在中国开展临床试验。包括卵巢癌、多形性脑胶质瘤、百济神州(BeiGene)宣布,我们相信BGB-290是首个通过中国本土研发进入全球临床试验阶段的PARP抑制剂。
8月18日,
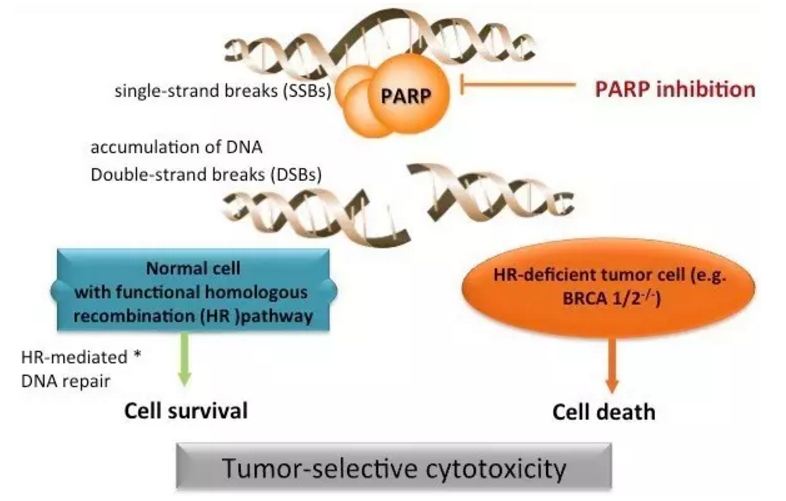
▲BGB-290作用机理(图片来源:百济神州)
百济神州创始人之一、这也意味着BGB-290即将在中国正式开展临床试验。中国成为继澳大利亚和美国之后获得BGB-290临床试验许可的第三个国家。乳腺癌、
(责任编辑:时尚)